1月6日,苏州泽璟生物制药股份有限公司(以下简称:泽璟制药)发布科创板上市招股意向书、上市发行安排及初步询价公告,这标志着科创板首家未盈利企业正式进入上市关键环节。此前的2018年10月30日,泽璟制药正式通过上交所上市委审核,成为目前第一家使用科创板第五套标准成功过会的医药企业。

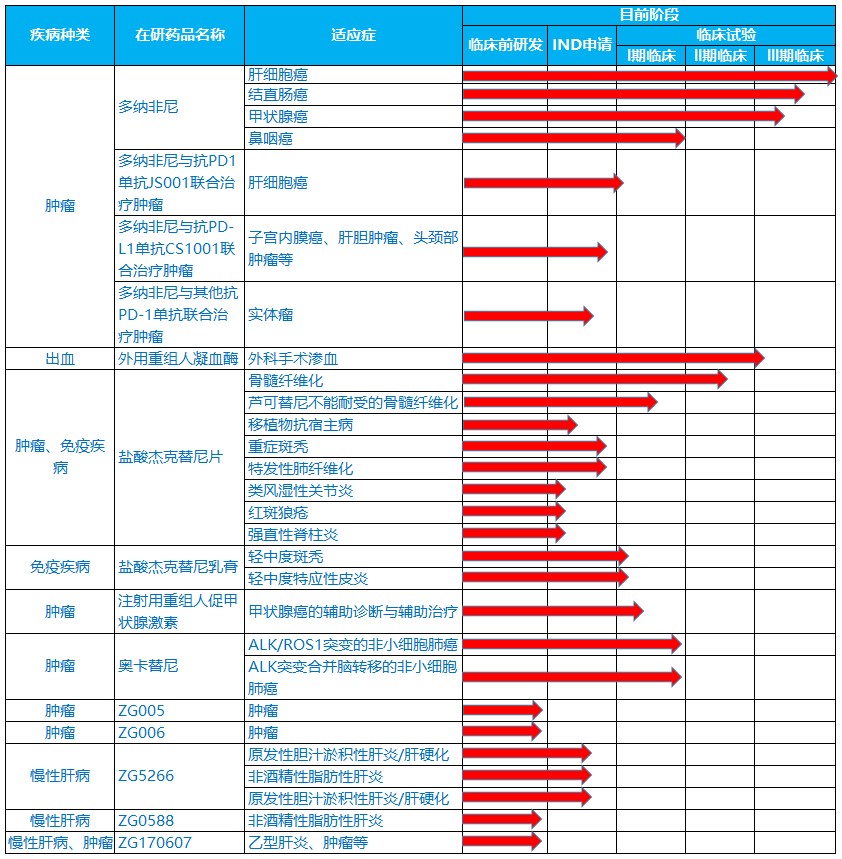
招股书显示,泽璟制药于2009年成立,实际控制人为盛泽林、陆惠萍,是一家专注于肿瘤、出血及血液疾病、肝胆疾病等多个治疗领域的创新驱动型新药研发企业。泽璟制药目前正在开发11个创新药物,其中甲苯磺酸多纳非尼片、重组人凝血酶及盐酸杰克替尼片已分别处于II/III期临床试验阶段。
招股书显示,报告期内,2016年至2019年1-6月,泽璟制药投入的研发费用分别为6107.74万元、1.59亿元、1.43亿元、7571.06万元,其中在研项目进入III期临床试验阶段后的研发费用占当年研发费用的比重分别为63.29%、47.22%、41.01%及18.07%。此次IPO,泽璟制药计划发行不超过6000万股,募集资金投入新药研发项目、新药研发生产中心二期工程建设项目、营运及发展储备资金。
泽璟制药的顺利上市与此次科创板改革密不可分。与主板、中小板、创业板不同,科创板不再设置单一、硬性的盈利及营收指标,引入市值概念,并结合市值、净利润、营业收入、现金流等内容创新设置了多元的财务指标。在其现有五套上市标准中,以第五套标准最为特殊,其完全与财务指标脱钩,转而用“预计市值不低于人民币40亿元,主要业务或产品需经国家有关部门批准,市场空间大,目前已取得阶段性成果(如Ⅱ期临床)、明显技术优势”等比较软性的要求,实际上大幅降低了企业上市标准。
因为第五套标准与生物科技企业创新研发周期长、投入大且早期无盈利的特点存在高度适应关系,市场普遍认为是为给生物科技企业量身定制。通常情况,一款新药的研发周期达7-10年,需经历药物发现、临床前研究、I-III期临床试验的漫长流程,最后经监管部门批准后方可上市,资金投入达1-10亿,而产品一旦上市则可收获高额销售回报,是典型的“高投入、高风险、高回报”行业。
新药研发的特性决定了其高度依赖外部融资。在美国,围绕新药研发企业已经形成一套完整资本市场支撑体系,覆盖了企业从早期天使融资到后期上市各个阶段,其中处于最后端也是最核心的环节便是纳斯达克。纳斯达克原则上不对公司的盈利、管理等实质性内容设置门槛,仅关注公司“是否披露了所有投资者关心的信息”,并确保信息的逻辑性、完整性、客观性、相关性。纳斯达克不仅为众多生物医药公司提供了重要的融资窗口,也为早期投资人提供了关键的退出渠道,进一步促进了对于早期研发的投资热情,早就了美国繁荣的生物医药投资。
反观国内,长期以来,受限于IPO对于盈利的硬性要求,初创型医药研发企业的国内上市之路困难重重,只有少部分幸运儿能够获得海外资本市场融资或被大公司收购的机会,对于投资退出的担忧极大限制了资本机构的参与热情,并进一步制约了产业的发展。直至本次科创板第五套申报标准的确立,初创型创新药企业在国内资本市场上市之路终于明朗,泽璟制药的顺利上市则证明了该路径的可行性,而且相比于其他地区资本市场,科创板在A股市场在估值、流动性以及提升企业知名度具有显著优势。我们认为,这将极大地激发投资机构对该赛道的投资热情,显著改善新药研发企业的融资环境,对于促进生物医药行业高质量发展具有里程碑意义。